

Псориаз – яркий пример сотрудничества между клиницистами и учеными в попытке найти безопасные и эффективные методы лечения о генетические расстройства кожи, суставов и иммунной системы. В некоторых случаях случайные клинические наблюдения приводили к лабораторной работе, которая объясняла патогенез этого расстройства; в других случаях терапия была основана на успешных эксперементах в лаборатории.
Результатом стало резкое улучшение нашего понимания патогенеза этого расстройства и нашей способности лечить пациентов, стражающих от псориаза. В статье estet-portal.com вы сможете ознакомиться с этапами раскрытия секрета патогенеза псориаза.
Первая причина псориаза – аномальная пролиферация кератиноцитов
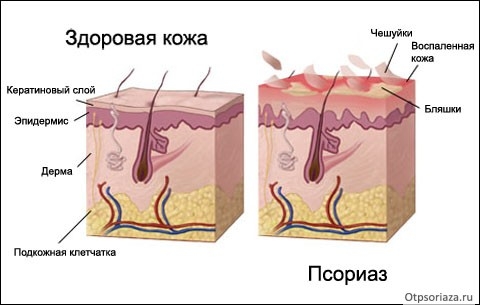
Сначала считалось, что псориаз является основным расстройством кератиноцита. В 1968 г. Вайнштейн, ван Скотт и Фрост демонстрировали аномальную пролиферацию кератиноцитов при псориазе. Было показано, что десквамация псориатического эпидермиса заметно быстрее, чем обычного эпидермиса.
Одновременно ван Скотт, Ауэрбах и Вайнштейн показали, что метотрексат эффективен при псориазе, предположительно, путем угнетения быстро делящихся эпидермальных клеткок.
В 1977 г. Пэрриш, Фицпатрик и его коллеги представили комбинацию псоралена и лечение ультрафиолетовой световой терапией (ultraviolet A – UVA) (фотохимиотерапия – PUVA). В 1979 г. было высказано мнение, что PUVA сшивает нити ДНК, и основной эффект вновь заключается в ингибировании пролиферации кератиноцитов.
Только спустя годы мы оценили влияние метотрексата и PUVA на иммунную систему.
Смотрите самые интересные видео на нашем канале в Youtube
Вторая причина псориаза – пролиферация кератиноцитов и активация Т-лимфоцитов
Вовлечение иммунной системы в патогенез псориаза было впервые оценено в 1988 г. в результате случайного наблюдения, что у пациентов с трансплантацией, у которых был псориаз и которые лечились циклоспорином, наблюдался регресс кожного заболевания. Гриффитс и Вурхи были одними из первых (1990 и 1989 гг. соответственно), отметивших, что благоприятный эффект циклоспорина на псориаз объясняется воздействием препарата на Т-лимфоциты.
Циклоспорин уменьшает количество иммунных клеток, включая Т-лимфоциты, моноциты, макрофаги и антигенпредставляющие клетки.
В 1990 г, работая со знаменитой группой ученых, Готлиб и Николофф и Гриффитс продемонстрировали много изменений в иммунной системе от циклоспориновой терапии и предположили, что при активации Т-клеток пораженные Т-клетки высвобождают лимфокины, способствующие пролиферации кератиноцитов.
Третья причина псориаза – активация Т-лимфоцитов
Роль лимфоцитов была убедительно подтверждена, когда в 1995 г. группа, возглавляемая Джеймсом Крюгером, успешно лечила псориаз с использованием лимфоцитарно-селективного слитого белка, состоящего из интерлейкина-2 и фрагментов дифтерийного токсина.
Последнее соединение селективно блокирует активированные лимфоциты, но не влияет на кератиноциты.
Восемь из 10 пациентов, получавших две дозы этого слитого белка, имели умеренное и значительное улучшение, подтверждая роль лимфоцитов.
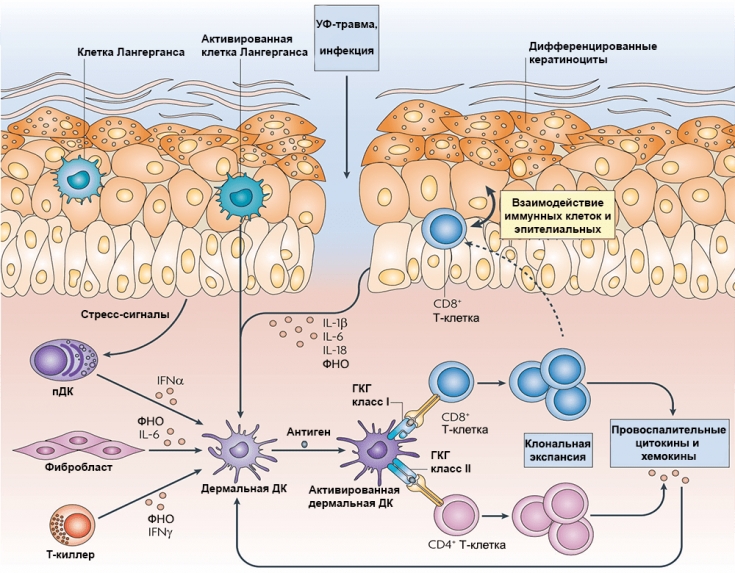
Было известно, что активация Т-клеток требует не только представления антигена Т-клеткам, но и костимуляции с рядом возможных сигналов.
CTLA-4 иммуноглобулин, теперь известный как препарат Абатацепт, представляет собой слитый белок, состоящий из Fc-части человеческого IgG1, слитого с внеклеточным доменом CTLA-4 (цитотоксический T-лимфоцит-ассоциированный антиген-4). Связываясь с молекулами B7 антигенпредставляющих клеток, Абатацепт предотвращает костимуляторный сигнал, тем самым блокируя активацию Т-клеток и приводя к улучшению состояния пациентов с псориазом.
Абатацепт одобрен для лечения ревматоидного артрита, все еще рассматривается в качестве лечения псориаза и псориатического артрита.
Читайте нас в Telegram
Четвертая причина псориаза – производство провоспалительных цитокинов
Роль цитокина Th1, IFN-γ, была признана в 2001 г. Считалось, что в этой сети цитокинов важную роль играет активация лимфоцитов и Т-клеток.
После клинических наблюдений в 2005 г. было доказано, что антагонисты TNF-α приводят к уменьшению IL-1 и IL-8 с последующим снижением экспрессии воспалительных генов, включая IFN-γ, Stat-1 и granzyme B. Антагонист интегрина αlβ2 эфализумаб также мешал работе Т-клеток в воспаленной коже.

Нестле и Конрад еще в 2004 году указывали, что p40 играет важную роль в псориазе. Это привело к развитию двух антител, нацеленных на p40 Устекинумабу и Бриакинумабу. Оба биологических агента, которые нацелены на компоненты p40 IL-12 и IL-23, были значительно эффективны, но из-за небольшого увеличения инфарктов миокарда в основных исследованиях одобрение бриакинумаба не проводилось.
В 2009 г. мы узнали, что IL-23 активирует клетки Th-17 для создания большего количества ИЛ-17. Клинически изучали по меньшей мере три антитела, нацеленные на IL-17 или его рецептор. Первый из них, недавно одобренный Сеукинумаб нацелен на IL-17A и оказался чрезвычайно эффективным при лечении псориаза в 2014 г. Иксекизумаб – еще одно антитело к IL-17A, является одинаково эффективным, как и бродалумаб, антитело к рецептору IL-17.
Перспективы дальнейших исследований
За последние пять десятилетий, успехи в нашем понимании и лечении псориаза вызваны тесным сотрудничеством между учеными и клиницистами, что делает псориаз моделью болезни, когда основным ученым и клиницистам лаборатории выгодно взаимодействовать друг с другом. Достижения в лаборатории перевели на новые методы лечения, которые являются более целенаправленными, глубоко эффективными и более безопасными, чем более старые методы лечения. Следующий рубеж при псориазе, вероятно, будет включать фармакогеномику или, в отдаленном будущем, даже генную терапию.
В 2001, 2007 и 2010 г. были созданы работы по идентифицированию генов, связанных с псориазом.
Спасибо, что остаетесь с estet-portal.com. Читайте другие интересные статьи в разделе «Эксперты». Возможно Вас заинтересует Лечение псориаза: опыт применения витамина D
По материалам Journal of Investigative Dermatology







Добавить комментарий