

Стволовые клетки регенерируют ткани в условиях гомеостаза и при стрессе. Принимая сигналы от их микроокружения, они плавно переходят из состояния покоя в активацию. Иммунные клетки выступают в роли помощников стволовых клеток по всему телу.
Здесь мы исследуем контекстно-специфические взаимодействия, которые стволовые клетки имеют с резидентными клетками и рекрутированными иммунными клетками (клетки врожденной иммунной системы, такие как макрофаги и дендритные клетки, а также адаптивные иммунные Т-клетки).
Читайте в статье estet-portal.com об этом увлекательном перекрестном контроле, который имеет большие перспективы для новых методов лечения воспалительных заболеваний и регенеративной медицины.
Роль стволовых клеток в механизмах самообновления
Самообновляющиеся тканевые стволовые клетки связаны с уравновешиванием пролиферацией и дифференцировкой, которая поддерживает равновесие между гиперплазией и атрофией. Скорость замены клеток во время гомеостаза зависит от тканей и фона.
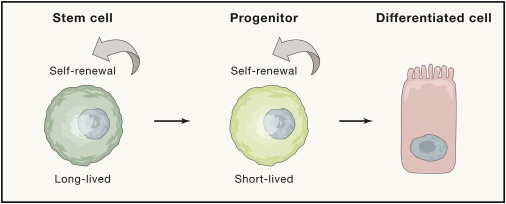
Процесс обновления непрерывен в крови, эпидермисе и кишечнике; ограничен в мозге и мышцах; и эпизодический в волосяном фолликуле и лактирующей молочной железе. Однако, когда ткани повреждены, стволовые клетки могут быть мобилизованы в действие в экстренном порядке. Наибольшая иммунная активность наблюдается в эпителиальных тканях кожи, легких и кишечника.
Смотрите самые интересные видео на нашем канале в Youtube
Роль иммунной системы в координации работы стволовых клеток
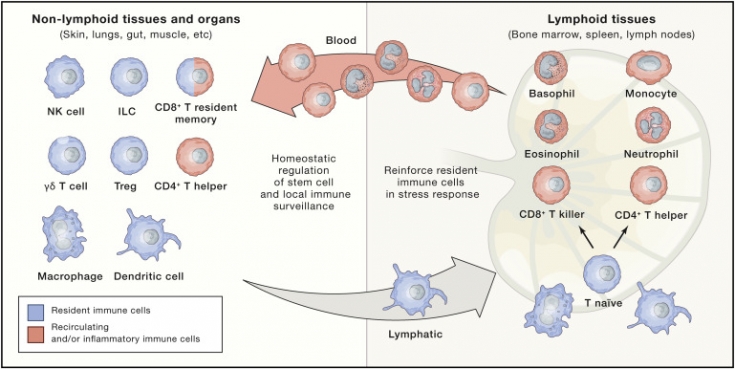
Иммунные эффекторы быстро поступают из сосудов, проникают в стрессовую ткань, чтобы очистить ее от проникающих патогенов, помочь в восстановлении гомеостаза.
Иммунитет кожи: нюансы о которых раньше не знали
Два устойчивых к тканям типа иммунных клеток - макрофаги и регуляторные Т-клетки (Tregs) - стали мощными регуляторами стволовых клеток в нормальных физиологических условиях. Макрофаги, классически известные как профессиональные фагоциты благодаря их способности поглощать мертвые и умирающие клетки, были в числе первых идентифицированных типов иммунных клеток, способных модулировать стволовые клетки. В костном мозге макрофаги регулируют сохранение гемопоэтических стволовых клеток (HSC).
Переход стволовых клеток фолликула между фазами телогена и анагена
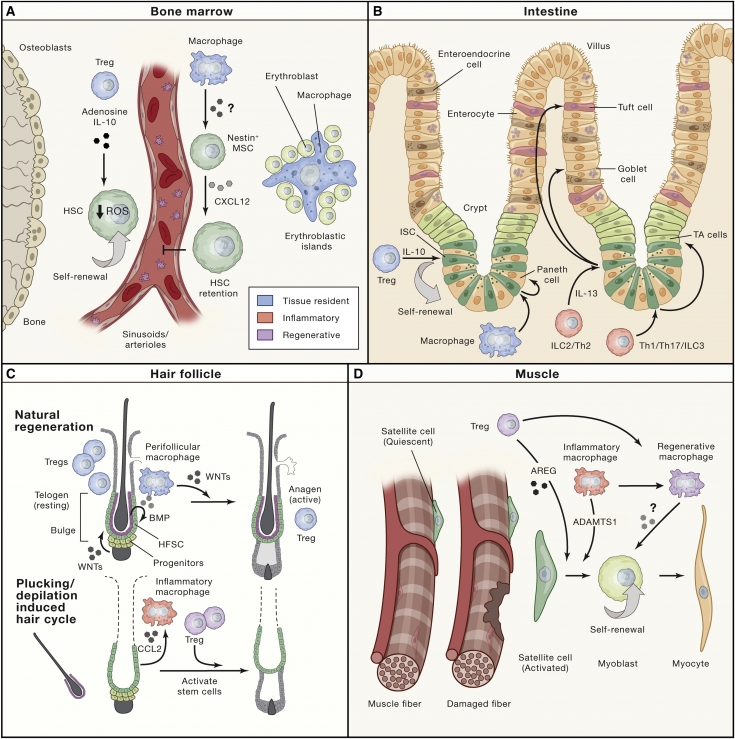
Фолликулы в коже необычны в том, что они подвергаются естественным циклическим фазам покоя (телоген) и регенерации (анаген). Соответственно, стволовые клетки, которые подпитывают этот процесс, переходят от покоящихся к активно работающим и обратно, поскольку они приводят к появлению более короткоживущих пролиферативных предшественников (транзитных амплифицирующих клеток), которые стимулируют периодическое восстановление волосяного фолликула, а также 7 дополнительных эпителиальных клеточных линии, которые формируют волос и его канал.
Активация этого естественного циклического регенеративного процесса требует изменений в нише стволовых клеток и включает в себя как подавление сигналов покоя (dampening of quiescence signals – BMP), так и увеличение активации стволовых клеток и регенеративных сигналов (WNT).
В то время как происхождение сигналов покоя было приписано терминальному дифференцированному потомству стволовых клеток (BMP), которые выстраивают линию «внутренней ниши», а также сигналы длинного диапазона от дермы; резонансные макрофаги были идентифицированы как активаторы стволовых клеток.
Во время прогрессирования от покоя до регенеративных фаз макрофаги собираются вокруг фолликула. Эти перифолликулярные макрофаги отмирают и высвобождают WNT7b и WNT10a для активации стволовых клеток волосяных фолликулов (hair follicle stem cells – HFSC).
Скоординированная работа – залог успешной активации стволовых клеток
Таким образом, физиологический процесс перехода из периода телогена к анагену включает множество молекулярных и клеточных механизмов, координация которых осуществляется благодаря сбалансированному взаимодействию стволовых клеток и клеток иммунной системы.
В этой связи существует три очевидных способа использования этих взаимодействий для терапевтической пользы:
1. усиление иммунных медиаторов для содействия регенерации,
2. исправление иммунных аномалий, лежащих в основе дегенерации тканей,
3. прерывание этого диалога для ограничения патологий в аутоиммунных.
Спасибо, что остаетесь с estet-portal.com. Читайте другие интересные статьи в разделе «Трихология». Возможно Вас заинтересует Анагеновая алопеция: причины и лечение
По материалам Cell







Добавить комментарий